Al inicio del siglo XXI, el Proyecto del Genoma Humano permitió conocer el texto completo de lo que algunos llaman el libro de la vida. Hoy se calcula que por cada dólar invertido ha habido un rendimiento de 141 dólares (la inversión fue de cerca de usd 10 mil millones). La genómica, orientada inicialmente al cuidado de la salud, ha encontrado terreno fértil para sus aplicaciones en agricultura, ganadería, energía, comercio y medio ambiente, donde ya genera crecimiento económico. La Organización para la Cooperación y el Desarrollo Económico (OCDE) la señala como uno de los principales motores de la bioeconomía. México puede sumarse a ella.

Hace poco más de 10 años, el 14 de marzo de 2000, el Presidente Clinton de Estados Unidos y el Primer Ministro Blair del Reino Unido anunciaron conjuntamente la publicación del primer borrador del genoma humano y un mapa que ubicaba a los genes que ahí se albergan.1,2 Así, el Proyecto del Genoma Humano logró la primera lectura de la cadena de 3 mil 200 millones de bases o nucleótidos —Adenina [A], Guanina [G], Timina [T] y Citosina [C]— que forman el genoma humano. Esta molécula de ácido desoxirribonucleico (ADN) tiene una estructura que semeja a una doble hélice y se alberga en el núcleo de cada una de las células del cuerpo humano. Su secuencia contiene cerca de 23 mil genes, segmentos del genoma que contienen instrucciones para que las células produzcan proteínas con funciones específicas para llevar a cabo los procesos químicos y formar las estructuras necesarias para la vida.
Análisis subsecuentes revelaron que 99.8% del genoma de un ser humano es idéntico al de cualquier otro; el resto corresponde a variaciones en la secuencia. Existen diferentes tipos de estas variaciones. Las más frecuentes corresponden a cambios de un solo nucleótido, conocidas como SNP’S (Single Nucleotide Polymorphisms, por sus siglas en inglés). Cada una ocupa un locus (del latín locus, lugar; loci en plural), es decir, una posición fija en la cadena. Esto significa que hay diferentes loci a lo largo de la cadena en que un nucleótido, por ejemplo A (AATAAAGGAAATAAA ACTTTTACT), varía al compararse con el nucleótido de otro individuo en la misma posición, por ejemplo G (AATA AAGGAAATGAAACTTTTACT). Si bien hasta el momento se han descubierto más de 15 millones de SNP’S en el genoma humano,3 cada individuo tiene cerca de 3 millones de loci en los cuales su secuencia varía con respecto a la secuencia de la mayoría de los miembros de su especie. Podríamos imaginar el conjunto de variaciones en el genoma de una persona como una huella que identifica a cada individuo. El conjunto de las variaciones del genoma humano forma una combinación única que le confiere individualidad genómica; la interacción de ésta con el medio ambiente define los rasgos físicos y químicos de cada uno. Dichas variaciones contribuyen a definir la predisposición o resistencia a enfermedades comunes, así como la respuesta a estímulos ambientales como los fármacos. Por ello, la culminación del Proyecto del Genoma Humano pronosticaba que vendrían avances de gran impacto para el cuidado de la salud pues se conocería el componente genético de las enfermedades humanas y se desarrollarían nuevas formas de prevención y tratamiento.
La generación vertiginosa de información genómica ha incrementado exponencialmente el conocimiento de los genes, las proteínas y sus funciones, y ha estimulado la generación de nuevas tecnologías, cada vez más eficientes, para la lectura y análisis genómicos. Más aún, su uso generalizado ha permitido la convergencia de tecnologías, especialmente aquellas de las ciencias de la vida y la ingeniería, logrando sus primeras aplicaciones funcionales a través de biología sintética (http://syntheticbiology.org/), capaz de generar organismos con funciones específicas, como la producción de medicamentos o combustibles, o bien la detección y destrucción de contaminantes en el medio ambiente.4
La capacidad de la genómica para transformar la información en conocimiento y el conocimiento en aplicaciones comienza a traducirse en la generación de valor y riqueza. Así sucede en actividades económicas que abarcan el cuidado de la salud, la agricultura, la ganadería, la industria y el medio ambiente.5 El impacto de estas áreas en la economía global comienza a posicionar a la genómica como un importante motor de la economía del conocimiento, cuya esencia es la participación del conocimiento en la competitividad y el desarrollo sustentable.6
La genómica en el desarrollo económico global
La economía del conocimiento es aquella cuyo funcionamiento se sustenta de manera predominante en la producción, distribución y uso del conocimiento y la información. Actualmente, más de 50% de Producto Interno Bruto (PIB) de las principales economías de la OCDE se basa en conocimiento.7,8 A diferencia de una economía tradicional, en una economía del conocimiento la información y la tecnología no son factores externos a los procesos de la producción, sino que influyen de forma directa en ellos. Así, a medida que las empresas adoptan insumos de conocimiento, se incrementa la demanda de empleados más calificados, se adoptan nuevas tecnologías y se generan paulatinamente nuevos conocimientos que son susceptibles de incorporarse en el proceso productivo. Las inversiones en conocimiento resultan claves para el crecimiento económico de largo plazo pues se caracterizan por incrementar los rendimientos. A diferencia de la economía convencional, en la cual el aumento de la inversión en capital, trabajo y materias primas llega al punto de disminuir su rendimiento, en las economías, industrias y empresas basadas en el conocimiento ocurre lo contrario: conforme aumenta la inversión en el conocimiento, el rendimiento no tiende a disminuir, sino que se incrementa.7
La economía basada en la invención, desarrollo, generación y uso de productos y procesos biológicos se conoce como bioeconomía. De acuerdo con la OCDE, su vertiginoso desarrollo ya le otorga un importante papel en el crecimiento económico tanto de países industrializados como de aquellos que están en proceso de serlo. Se prevé que estos beneficios tengan un impacto sensible en el cuidado de la salud, la productividad en la agricultura9 y la ganadería, el desarrollo industrial y la remediación del medio ambiente. Sin embargo, el desarrollo pleno de la bioeconomía requiere de la implementación de políticas coordinadas de los gobiernos que estimulen y protejan cada uno de los pasos de la cadena de valor, desde la investigación y el desarrollo hasta la colocación de los productos en el mercado.
La OCDE señala que para el año 2030 la bioeconomía incluirá entre sus ejes centrales al conocimiento avanzado de los genes y los procesos celulares complejos, la capacidad de generar biomasa renovable y la integración transversal de las aplicaciones biotecnológicas en diversos sectores.10 Esta predicción es congruente con el rápido avance científico y tecnológico detonado por el desarrollo de las ciencias genómicas cuyo impacto en el ámbito económico es cada vez más evidente. Si bien hace apenas unos años las aplicaciones prácticas de la genómica en la vida cotidiana se veían lejanas, hoy ya existen algunas muy claras. Más aún, actualmente no sólo se reconoce el poder transformador de la genómica, sino que también comienzan a surgir mecanismos para otorgarle valor económico a sus aplicaciones en el contexto de la economía del conocimiento.11

Simultáneamente, organizaciones como la OCDE trabajan en la generación de principios y buenas prácticas que contribuyan a regular la participación de la genómica en la economía contemporánea y la implementación de nuevos modelos de participación del Estado que estimulen y normen su desarrollo. Así, la OCDE destaca la importancia de diseñar una agenda de políticas públicas orientadas a favorecer la generación de beneficios sociales, ambientales y económicos a partir de tecnologías basadas en evidencia científica y enfocadas a atender grandes retos como la suficiencia alimentaria, el cuidado de la salud y el desarrollo industrial.10
El creciente interés en las implicaciones de la genómica para la bioeconomía llevó a la OCDE y a la Organización del Genoma Humano (HUGO, por sus siglas en inglés) a emprender un esfuerzo conjunto para analizar la situación actual de esa relación y definir sus alcances en el mediano plazo. Así, en mayo de 2010 realizaron conjuntamente un simposio sobre genómica y bioeconomía en Montpellier, Francia (http://www.bioeconomy2010.org/). En él, líderes mundiales de las diversas áreas de la genómica se dieron cita para revisar las principales aplicaciones comerciales existentes y otras en proceso de desarrollo. Además, se identificaron indicadores para medir el impacto de esas aplicaciones, políticas públicas posibles que contribuyan a superar exitosamente los retos inherentes a su implementación, mecanismos de acceso a capitales adecuados y estrategias relacionadas con la propiedad intelectual, entre otros temas relevantes. A este esfuerzo se sumaron el Centro para la Salud Global de la Universidad de Toronto y la Fundación Mexicana para la Salud (FUNSALUD). Más adelante, en diciembre de 2010, se llevó a cabo el Foro Global de Biotecnología en la sede de la ocde en París, en conjunto con el Consejo de Investigación Económica y Social del Reino Unido (http://www.oecd.org/document/8/0,3746, en_2649_34537_ 46142664_1_1_1_1,00.html). Este esfuerzo permitió analizar desarrollos genómicos cuyo diseño se vincula con el progreso económico, identificando las fortalezas y los retos que enfrentan estos modelos emergentes. Estos trabajos iniciales hicieron evidente que si bien el desarrollo de las plataformas tecnológicas y la generación de información genómica ha sido de considerable magnitud, sus aplicaciones directas son limitadas, por lo cual es indispensable el desarrollo de nuevas estrategias que estimulen la innovación para generar un verdadero impacto en la economía global. Uno de los modelos propuestos es la convergencia de disciplinas tradicionalmente distantes. Así, en marzo de 2011, la HUGO y la OCDE llevaron a cabo la reunión internacional Converging Technologies in Genomics: Opportunities for a Global Economy, en Dubai, Emiratos Árabes Unidos (http://www.hgm2011.org/schedule_-_day_2_-_15_march.html), con el fin de contribuir a identificar factores estratégicos para la integración plena de la genómica a la economía global.
Las evidencias generadas a partir de estos esfuerzos iniciales dieron lugar a que la hugo estableciera formalmente un Comité de Genómica y Bioeconomía como parte formal de su estructura (http://www.hugo-international.org/comm_genomicsandbioeconomy.php). Por otra parte, su Consejo Directivo decidió llevar a cabo, en conjunto con la ocde, una reunión para dar a conocer este proyecto en México, así como para integrar esta área al programa científico de la Reunión Anual del Genoma Humano en Sidney, Australia, en 2012.
El poder transformador de la genómica
La genómica comienza a convertirse en uno de los principales motores del crecimiento económico en el contexto de la bioeconomía. Su desarrollo guarda paralelismos con la época en que los transistores y los circuitos integrados transformaron radicalmente la economía y la sociedad. Actualmente no hay segmento de la economía que no dependa de estos componentes electrónicos. Su empleo en la construcción de computadoras sentó las bases para crear el internet. Así, componentes tecnológicos fundamentales como los circuitos integrados, al agregarse a un aparato de mayor grado de complejidad, por ejemplo las computadoras, pueden generar una oportunidad económica totalmente nueva como lo ha sido el internet. De forma similar, la disponibilidad de tecnología para secuenciar y sintetizar genomas ofrece la posibilidad de integrar sistemas más complejos orientados a la generación de aplicaciones que contribuyan al desarrollo económico global.
A 10 años de la secuenciación del genoma humano, ha quedado claro que el Proyecto del Genoma Humano ha transformado a la genómica en un importante motor de la economía contemporánea. El reporte El impacto económico del Proyecto del Genoma Humano, publicado recientemente por el Battelle Memorial Institute de Estados Unidos, muestra que el rendimiento de la inversión en genómica ha sido de 141 dólares por cada uno de los casi 5 mil 600 millones invertidos en su desarrollo inicial, y que hoy llegan a cerca de 10 mil millones (http://www.battelle.org/publications/humangenomeproject.pdf). Sólo en 2010, los proyectos de secuenciación genómica y las actividades industriales y de investigación asociadas a ellos generaron 67 mil millones de dólares, 20 mil millones de dólares en ingresos entre trabajadores de Estados Unidos y 310 mil empleos.
Lo anterior es congruente con algunas tendencias actuales que muestran el impacto que la genómica comienza a tener en la economía, entre ellas la curva de abatimiento en el costo de la secuenciación genómica (ver Figura 1),12 el incremento en el descubrimiento de loci asociados al riesgo de padecer enfermedades comunes13 o de sufrir efectos adversos a los medicamentos, el incremento en el número de pruebas de diagnóstico genético y el incremento de políticas públicas relacionadas con la información al público sobre biomarcadores genómicos asociados a reacciones adversas a los medicamentos,14 así como la implementación del uso de marcadores genéticos para definir las mejores cruzas en la industria ganadera,15 el desarrollo de más y mejores cereales16 y otros alimentos, mejorados a través de la selección genética, y el surgimiento de tecnologías innovadoras como la biología sintética para la producción de moléculas de alto valor económico.4
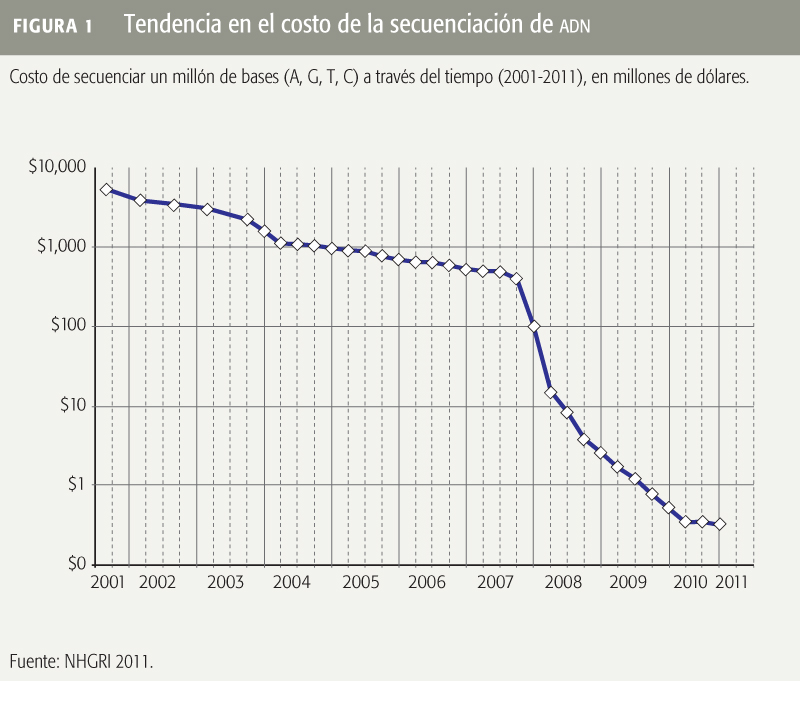
Las plataformas tecnológicas para la secuenciación de ADN han evolucionado hacia modelos cada vez más eficientes que abaten los costos en forma considerable y que, en consecuencia, hacen cada vez más accesible la secuenciación de genomas completos. La secuenciación del primer genoma humano tuvo un costo de más de 3 mil millones de dólares. Hoy, en cambio, existen decenas de laboratorios en el mundo que secuencian genomas completos cotidianamente a un costo menor a 50 mil dólares por cada uno, y muy pronto se espera lograrlo por menos de mil dólares,12 lo que hace evidente que en un futuro cercano la secuencia del genoma individual será parte rutinaria del cuidado de la salud.17
Las aplicaciones médicas de la genómica tienen especial vigencia para la medicina genómica, es decir, el cuidado de la salud basado en la información del genoma de cada persona. Su desarrollo permitirá una práctica médica más individualizada, más predictiva y más preventiva.18 La importancia estratégica de la medicina genómica ha sido plenamente reconocida por la Organización Mundial de la Salud (OMS).19 El camino hacia este nuevo paradigma en el cuidado de la salud ha registrado avances importantes, y si bien existen aún metas por cumplir, alcanzarlas será sólo cuestión de tiempo.
El análisis comparativo de múltiples genomas incrementó de manera exponencial el conocimiento de las variaciones genéticas que predisponen a enfermedades comunes. En el año 2000, además de aquellas del locus hla, sólo una docena de ellas se había asociado consistentemente a la predisposición a alguna de estas enfermedades. Una década después, se han identificado más de 1,100 loci que contribuyen a más de 165 enfermedades y rasgos asociados con enfermedades comunes. Casi todos ellos fueron identificados a partir de 2007 mediante el estudio de poblaciones utilizando nuevas tecnologías genómicas e informáticas. A partir de estos estudios se ha demostrado que la mayor parte de los rasgos puede ser influenciada por un gran número de loci y que la gran mayoría de las variaciones comunes tiene un efecto moderado, con un incremento en el riesgo de entre 10 y 50% (similar al de los efectos de muchos factores de riesgo ambiental).13 En consecuencia, el número de pruebas de diagnóstico genético en el mercado ha tenido una tendencia ascendente sostenida: se ha triplicado en la última década. Actualmente existen más de 2 mil pruebas genéticas en el mercado (http://www.ncbi.nlm.nih.gov/sites/genetests/?db=genetests). Más aún, las nuevas tecnologías de secuenciación permiten la identificación precisa y rápida de gérmenes causantes de infecciones humanas20-22 y el desarrollo de aplicaciones concretas para el diagnóstico de estos importantes problemas de salud.
El conocimiento de estas variaciones genéticas permitirá mejores acciones para la prevención y el manejo de un gran número de enfermedades comunes, con base en las características y predisposiciones individuales.23 Algunas de las aplicaciones prácticas del conocimiento del genoma humano consisten en identificar a aquellos individuos cuyo contacto con determinados fármacos les desencadenará reacciones adversas que pueden poner en riesgo la función de sus órganos o incluso su vida. Esta disciplina se conoce como farmacogenómica.24,25 Las evidencias científicas comienzan a incidir sobre políticas públicas en beneficio del consumidor. Actualmente, la Food and Drug Administration (FDA) de Estados Unidos ha reconocido la importancia de diversos marcadores genómicos y ha emitido regulaciones que hacen obligatorio incluir esta información en las etiquetas de más de 75 medicamentos de uso común cuya dosis requiere ser ajustada en forma personalizada, de acuerdo a la presencia de determinadas variaciones genómicas (http://www.fda.gov/drugs/scienceresearch/researchareas/pharmacogenetics/ucm083378.htm). Más aún, se espera que en el futuro puedan diseñarse fármacos dirigidos a grupos poblacionales que compartan secuencias de adn asociadas a un mejor efecto y una menor toxicidad.14
La utilización de las plataformas tecnológicas en genómica se ha ampliado más allá del estudio del genoma humano. Actualmente se conoce la secuencia completa del genoma de más de 4 mil 400 especies diferentes, incluyendo animales, plantas, hongos, bacterias y virus26 (Figura 2). Así también, se han estudiado algunas especies en peligro de extinción como el orangután, el panda, el koala, el oso polar, el pingüino y los arrecifes de coral.
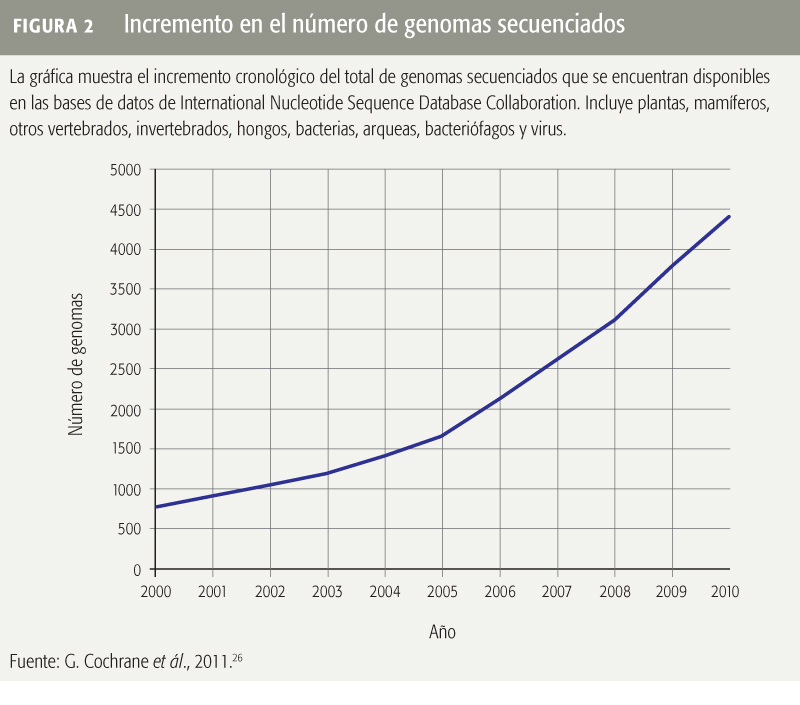
La secuenciación del genoma de especies de alto valor comercial como el ganado vacuno y el porcino y de aves de corral ha permitido desarrollar instrumentos para la identificación de variaciones de su genoma que determinan rasgos de alto valor económico.15,27,28 Estos avances han permitido la selección de colonias de ganado más robustas y más resistentes a enfermedades infecciosas. La información genómica comienza a utilizarse para identificar con precisión a una especie, su capacidad adaptativa, los contenidos nutrimentales de sus productos y, en consecuencia, para definir las cruzas de animales más efectivas a nivel comercial. Estas aplicaciones han reducido los tiempos para obtener animales con características deseadas por la industria.15,27
Los sistemas de identificación genómica se utilizan en el monitoreo de especies y plagas invasivas, vigilancia microbiológica del medio ambiente, seguridad de alimentos y combate contra el fraude comercial, pues permiten distinguir organismos en forma inequívoca y rápida. Una de sus aplicaciones ha encontrado un nicho de alto valor comercial en la industria pesquera de Estados Unidos; se calcula que entre 25 y 30% del pescado que se vende en ese país se etiqueta erróneamente como otro de calidad superior.29 Por ello, la FDA comienza a implementar un sistema de identificación genómico, equivalente a un código de barras, para el cuidado y fortalecimiento de esa industria (http://www.fda.gov/food/scienceresearch/laboratorymethods/ucm169034.htm). Este sistema ha sido desarrollado por el proyecto FISH-BOL (http://www.fishbol.org/) de la organización International Barcode of Life (http://ibol.org/), formada con el esfuerzo de varias naciones.
Las aplicaciones genómicas en las especies vegetales cobran particular importancia por su potencial contribución estratégica a la atención del reto de la suficiencia alimentaria para una población mundial que se incrementará en un tercio en los próximos 20 años, sobre todo en un planeta con serios retos ambientales que amenazan la supervivencia de las especies. Actualmente existe un gran número de especies vegetales cuyo genoma ha sido secuenciado, lo que permite la identificación inicial de variaciones genómicas asociadas a rasgos que afectan su valor comercial. Tal es el caso de diversos cultivos para el consumo humano en cuyos genomas comienzan a identificarse secuencias que definen sus características nutrimentales, su tolerancia a agresiones del medio ambiente y su capacidad productora de granos, entre otras.16,30
La convergencia del conocimiento y las tecnologías genómicas con la física y la ingeniería ha dado lugar a la biología sintética, que consiste en el diseño y construcción de nuevas partes biológicas, instrumentos y sistemas, así como el rediseño de sistemas biológicos ya existentes, ahora con fines prácticos. Algunos de estos desarrollos tienen el potencial de contribuir a enfrentar retos globales. Sus avances más recientes incluyen la construcción de los primeros genomas artificiales de microorganismos con funciones “bajo diseño”, como la remediación ambiental,31 y la producción de algunos medicamentos32 y de otras moléculas de alto valor comercial como biocombustibles.33,34 Estas aplicaciones en proceso de desarrollo han llevado a los países miembros de la ocde a analizar formalmente las oportunidades y retos que plantea este nuevo campo (http://www.oecd.org/document/8/0,3746,en_2649_37437_46142664 _1_1_1_37437,00.html), incluyendo los retos éticos y legales, que comienzan a ser estudiados por los gobiernos (http://www.bioethics.gov/documents/synthetic-biology/PCSBI-Synthetic-Biology-Report-12.16.10.pdf).
La bioeconomía requiere políticas públicas con visión de futuro
La transformación de la información genómica en bienes y servicios se monetizará, e identificará nuevos e insospechados mercados. Para lograrlo, será necesaria la sinergia creativa entre tecnologías y campos del conocimiento en el contexto de políticas públicas que favorezcan la generación de soluciones innovadoras orientadas a atender los retos más importantes para las sociedades. Pues así como la economía del conocimiento impone nuevas competencias relacionadas con las necesidades de la sociedad, también requiere de la capacidad de aprendizaje de las instituciones públicas y los sectores productivo y académico, y de la vinculación para la solución de problemas y el uso intensivo del conocimiento en el espacio social.
La bioeconomía ha generado nuevos retos en diversos ámbitos relacionados con su desarrollo. De ahí la necesidad de políticas públicas diseñadas con visión de futuro y orientadas a generar un entorno que favorezca la innovación basada en el conocimiento y su integración exitosa a la economía. Para ello, resulta fundamental (1) identificar cada uno de los elementos de la cadena de valor, (2) generar recursos humanos con conocimientos de frontera, (3) alinear la estructura de los modelos académicos y de las instituciones que generan la investigación científica con soluciones concretas a grandes retos con impacto económico, (4) asegurar el financiamiento suficiente y sostenido para investigación y desarrollo, y establecer criterios para la definición de prioridades en salud, agricultura e industria sobre los cuales deban concentrarse los esfuerzos en forma sostenida, así como (5) establecer un marco jurídico claro que estimule la integración de los resultados de la investigación y el desarrollo a la economía de cada nación, entre otras tareas.
Sin demérito de la investigación básica, que por sí misma tiene un valor intrínseco, y que nutre a la investigación aplicada, resulta importante establecer modelos académicos y de investigación innovadores que promuevan el desarrollo de aplicaciones prácticas con potencial valor comercial. Los estímulos y la remuneración de quienes desarrollan la investigación científica deben ser competitivos, y se deben definir los criterios para estimular esas actividades y su relación con propiedad intelectual competitiva.35,36 Por ello, es necesario que las políticas públicas que buscan dar más valor al conocimiento científico resulten de un esfuerzo concertado para hacer coincidir los marcos reguladores existentes con los avances de las ciencias de la vida y, cuando sea apropiado, para considerar la creación de otros nuevos.
Además de la infraestructura institucional, humana y física para la generación de nuevos conocimientos, es conveniente establecer los mecanismos adecuados para determinar su valor y buscar su integración a los procesos productivos donde resulte más útil, a fin de estimular la innovación. Para que esto suceda, las políticas públicas deben orientarse a estimular la innovación en ciencia y tecnología en forma competitiva y sostenida. Este proceso es complejo no sólo por el número de disciplinas e individuos que participan en él, sino por la gran cantidad de factores intrínsecos y extrínsecos que influyen su desempeño y sustentabilidad.11
La implementación exitosa del proceso innovador en ciencias de la vida requiere de políticas de Estado que reconozcan al conocimiento como motor de desarrollo social y económico de la nación bajo la forma de nuevos productos, servicios y desarrollos empresariales. En consecuencia, la participación del Estado debe orientar los esfuerzos para la creación de una plataforma de mediano y largo plazos que asegure la innovación en ciencias de la vida en torno a prioridades sólidamente fundamentadas. Para ello, comienzan a desarrollarse modelos innovadores de participación del Estado que integran esfuerzos en educación, desarrollo científico y tecnológico, protección de la propiedad intelectual, mecanismos públicos y privados para el financiamiento sostenido de la investigación científica y para su integración con el sector productivo, y mecanismos que permitan la participación de la sociedad en la definición de las prioridades en materia de investigación y desarrollo.
Actualmente, existen economías emergentes que han desarrollado exitosamente políticas de Estado orientadas a desarrollar estrategias para la competitividad en ciencia y tecnología en el contexto de la bioeconomía. Por ejemplo, China incrementó su inversión en ciencia y desarrollo 30% entre 2001 y 2006, y en 2010, el número de doctores en ciencias que formaron Brasil, China, India y Sudáfrica equivalió a la mitad de los que formaron los 34 países miembros de la ocde en su conjunto.37
La oportunidad de incorporar los desarrollos genómicos de México a la bioeconomía
La importante contribución de la genómica a diversas áreas de alto impacto económico y el liderazgo de la OCDE en esta materia ofrecen una valiosa oportunidad para aquellos países que cuentan con iniciativas robustas en ciencias genómicas.10 Éste es el caso de México, en donde la genómica ha sido uno de los campos de la ciencia cuyo desarrollo ha sido oportuno y con sólidas bases institucionales en las áreas médica, agronómica, ganadera e industrial.
En los últimos 20 años se han llevado a cabo importantes esfuerzos para el desarrollo de las ciencias genómicas en México. Por ejemplo, la participación en el proyecto del genoma de la bacteria Escherichia coli, así como la secuenciación del Rhizobium etli, realizada en el Centro de Ciencias Genómicas (antes Centro de Fijación de Nitrógeno) de la Universidad Nacional Autónoma de México (UNAM).38 Estos y otros proyectos dieron lugar a una serie de iniciativas genómicas relacionadas con diferentes organismos, como el parásito humano Taenia solium.39 El Centro de Investigación y de Estudios Avanzados del Instituto Politécnico Nacional (CINVESTAV) estableció el Laboratorio Nacional de Genómica para la Biodiversidad (LANGEBIO), que desarrolla programas sobre genómica en plantas, tales como la secuenciación y análisis funcional del genoma del maíz. Otros núcleos de desarrollo se han establecido en Guanajuato, Nuevo León, Jalisco, Tamaulipas y Yucatán, entre otros estados.40 En 2004, la UNAM creó la licenciatura en Ciencias Genómicas.41
El área médica no ha sido la excepción. Como parte de una larga tradición en genética humana,42 se han hecho esfuerzos multiinstitucionales para el desarrollo de una plataforma nacional en medicina genómica.43,44 Así, la labor que iniciaron en 2001 la Secretaría de Salud, la unam, el Consejo Nacional de Ciencia y Tecnología y la funsalud dio lugar a que el Congreso de la Unión modificara la ley para crear el Instituto Nacional de Medicina Genómica (INMEGEN), ratificado por el Presidente de la República el 20 de julio de 2004.45 Este proyecto ha dado lugar a una importante masa crítica de especialistas en la materia, infraestructura de vanguardia, programas de formación de recursos humanos y proyectos de investigación en medicina genómica que han sentado las bases para el desarrollo de esta especialidad en México.46 Entre dichos proyectos destaca el primer análisis de la diversidad genómica en poblaciones mestizas mexicanas (http://genomamexicanos.inmegen.gob.mx), conocido como el Mapa del Genoma de los Mexicanos. Elaborado por científicos mexicanos del inmegen, fue publicado por la Academia de Ciencias de Estados Unidos.47 Los logros alcanzados en medicina genómica han recibido el reconocimiento internacional, incluyendo el de la Organización Mundial de la Salud (http://www.who.int/genomics/professionals/applications/mexico/en/index.html).
México tiene la oportunidad de establecer un círculo virtuoso entre la investigación en ciencias genómicas y su desarrollo social, pues la inversión sostenida en investigación genómica dará lugar a un mayor conocimiento científico en un tiempo razonable y con la participación de las múltiples instituciones que la desarrollan en el país. Este conocimiento incidirá en tres áreas principales: el desarrollo tecnológico, la generación de evidencias y el empoderamiento de las personas para tomar decisiones sobre estilos de vida y entornos más sanos (ver Figura 3). A su vez, el desarrollo tecnológico bien orientado y apoyado de manera sostenida tiene el potencial de generar aplicaciones concretas para mejorar el cuidado de la salud, la productividad en la agricultura y la ganadería y el desarrollo industrial, en forma tal que contribuyan a la bioeconomía y consecuentemente al crecimiento económico del país.

La generación de evidencias científicas contribuirá, como lo ha hecho exitosamente en el pasado, al desarrollo de políticas públicas que fortalezcan la bioeconomía y el bienestar social. El conocimiento científico permite el empoderamiento por parte de las personas, lo que se traduce en conductas personales que favorecen estilos de vida más saludables y un mejor entorno ambiental, lo que fomenta un mejor cuidado de la salud. A su vez, estas acciones contribuyen a robustecer la seguridad alimentaria, ambiental e incluso energética, lo que también debe fortalecer la bioeconomía y generar una mayor inversión en investigación genómica.
Si bien este círculo virtuoso es deseable y redundaría en grandes beneficios sociales y económicos para México, su implementación requiere de una estrategia cuidadosamente diseñada, con pasos y metas claramente definidos, que incluya la participación de diversos sectores para el desarrollo de políticas públicas adecuadas, un financiamiento suficiente y sostenido y la implementación de vinculaciones estratégicas al interior y al exterior del país.
Por ello, los resultados del análisis que hizo la ocde en 2009 sobre el estado que guardan la ciencia, la tecnología y la industria en sus países miembros deben ser materia de seria reflexión, pues ofrecen evidencias de que en México existe un entorno poco apropiado para la innovación y el desarrollo de la bioeconomía, lo que inhibe la incorporación de los esfuerzos genómicos al desarrollo económico del país. Es así que, la incorporación de la genómica a la bioeconomía en México requeriría de cambios importantes en las políticas de Estado correspondientes.
México es el país miembro de la OCDE con la inversión más baja en investigación y desarrollo. Su gasto doméstico bruto en investigación y desarrollo (GERD, por sus siglas en inglés) equivalió a 0.4% del pib en 2007, y se mantuvo alrededor de este nivel entre 2000 y 2010. El GERD per cápita es también el más bajo de la OCDE. El gasto de sector empresarial en investigación y desarrollo fue de 0.2% del pib, lo que significa que se duplicó con respecto al año 2000, cuando era de 0.1%. Si bien los graduados de ciencias e ingeniería representaron 24.7% del total, por encima del promedio de la OCDE, hay menos de un investigador por cada mil empleos, lo que representa el promedio más bajo de la OCDE.37
En una economía como la de México —que atraviesa por cambios estructurales, con retos fundamentales que incluyen el mejoramiento del sistema educativo, la actualización de su infraestructura, la modernización del marco jurídico laboral y el estímulo de la inversión privada en diversos sectores—, la innovación puede tener un importante papel en beneficio de todas esas áreas. Sin embargo, los resultados que tiene México en innovación son muy limitados: la generación de 0.14 patentes y 73 artículos científicos por millón de habitantes fue la más baja de la ocde en 2008.37
La situación en los demás países miembros de la OCDE y en algunos países no miembros ha sido diferente. En ellos, la tendencia de la inversión en ciencia y tecnología como porcentaje del pib ha continuado incrementándose. Incluso en algunos de estos países ha sido muy significativo (ver la Figura 4). El incremento más importante se observó en China, donde se registró un aumento en la proporción gerd/pib de 135%, es decir, pasó de 0.65 a 1.54% de su pib. El aumento de esa proporción fue de 131% Portugal, de 95% en Turquía, de 55% en Israel y de 54% en España. México ocupó el último lugar, prácticamente sin cambios en la década reportada (1998-2008).37
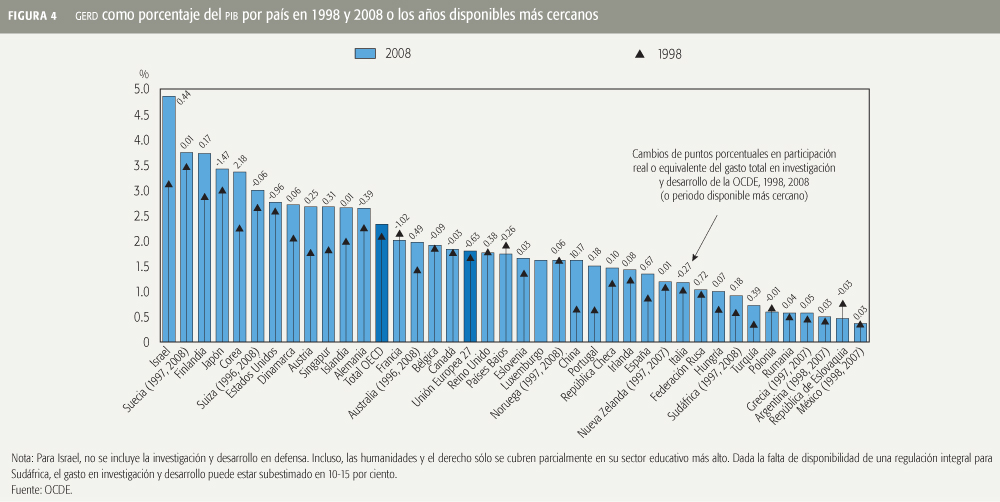
El reto clave para México es establecer las condiciones que fomenten la innovación a través de diversos canales, incluyendo la educación y el entorno competitivo y regulatorio. Las recomendaciones de la ocde en su Revisión de Políticas de Innovación en México 2009 incluyen el establecimiento de mejores estructuras para la participación del Estado, que aseguren la coherencia en la formulación e implementación de las políticas de innovación tanto a nivel federal como estatal, así como la inversión sostenida en investigación y desarrollo.8,48
Estrategia para la integración de la genómica a la bioeconomía en México
Las aplicaciones de la genómica en las actividades que rigen el desarrollo económico son cada vez más y de mayor relevancia. En parte, por su amplio espectro; en parte, por las sinergias que se establecen entre diversas disciplinas para lograr objetivos concretos que se traducen en aplicaciones de alto valor económico. En México, el desarrollo académico de las ciencias genómicas ha encontrado un terreno fértil, lo que ha dado lugar a sólidas bases que pueden contribuir al desarrollo de aplicaciones útiles para potenciar el crecimiento económico del país en el contexto de la bioeconomía.
La oportunidad de que México se beneficie de la bioeconomía a través de sus plataformas genómicas nos ha llevado a plantear la iniciativa “Genómica para el crecimiento económico de México”, que está orientada al análisis de los retos y oportunidades relacionados con la incorporación de la genómica al desarrollo económico. Se ha formado un grupo de trabajo que identificará oportunidades que vinculen la genómica con el sector productivo y propondrá mecanismos para estimular esta integración. Con este fin, el grupo de trabajo utiliza diversas metodologías para el planteamiento de acciones que busquen la integración de la genómica a la bioeconomía en México.
Los esfuerzos iniciales han dado lugar a la identificación de áreas de desarrollo genómico a nivel global que contribuyen al desarrollo económico, y al establecimiento de vinculaciones con las instituciones que las desarrollan y las personas que dirigen los proyectos. Además, se han establecido sinergias con instituciones como la OCDE, el HUGO y la Universidad de Harvard, cuya contribución al desarrollo de esta iniciativa será de la mayor relevancia. El siguiente paso será la ampliación del grupo de trabajo a fin de estimular su pluralidad mediante la integración de instituciones y personas cuyas contribuciones agreguen valor al proyecto. Así, se procederá a evaluar los elementos del proceso de innovación basado en la genómica, los diversos retos que enfrenta cada uno, el marco jurídico que los regula, las oportunidades para el desarrollo de iniciativas de alto impacto económico y los elementos necesarios para detonar sinergias estratégicas, entre otros aspectos.
Además, el proyecto contempla la formación de algunos núcleos de trabajo que lleven a cabo investigación sobre temas específicos. Se anticipa la realización de entrevistas, foros de consulta y otros eventos que contribuyan a nutrir esta iniciativa. Los resultados incluirán la generación de propuestas en torno a oportunidades concretas de integración de la genómica a actividades de alto valor económico y social.
El grupo de trabajo explorará diferentes fuentes de financiamiento potenciales para la conducción de estos trabajos, y evaluará el establecimiento de sinergias estratégicas que permitan incubar los primeros proyectos.
Hoy más que nunca, la genómica representa un activo importante para el crecimiento sostenido y la competitividad de las naciones. México debe estimular la generación de productos basados en la genómica que contribuyan al desarrollo económico. Su incursión en la bioeconomía, a partir de los desarrollos genómicos con que cuenta, le abrirá nuevas oportunidades para la competencia global. La suma de esfuerzos coordinados entre quienes generan información genómica y quienes desarrollan y comercializan nuevos productos ofrece la posibilidad de un círculo virtuoso. La vinculación entre los desarrollos genómicos y el sector productivo para generar aplicaciones innovadoras de alto valor comercial podría convertir la inversión que México ha hecho en genómica, en una de las más redituables para el país.
___________________________
GERARDO JIMÉNEZ-SÁNCHEZ es Presidente de Biotecnología de la Organización para la Cooperación y el Desarrollo Económico, Miembro del Consejo Directivo y Presidente del Comité de Bioeconomía de la Organización Mundial del Genoma Humano (HUGO, por sus siglas en inglés) y Presidente Consultivo de Global Biotech Consulting Group (GBC Group) ([email protected]). JULIO FRENK es Decano de la Escuela de Salud Pública de la Universidad de Harvard. GUILLERMO SOBERÓN es Presidente Emérito de la Fundación Mexicana para la Salud.
_____________________________________________
1 Lander, E.S. et ál., “Initial Sequencing and Analysis of the Human Genome”, Nature 409, 860-921, 2001.
2 Venter, J.C. et ál., “The Sequence of the Human Genome”, Science 291, 1304-51, 2001.
3 Durbin, R.M. et ál., “A Map of Human Genome Variation from Population-scale Sequencing”, Nature 467, 1061-73, 2010.
4 Andrianantoandro, E., S. Basu, D.K. Karig y R. Weiss, “Synthetic Biology: New Engineering Rules for an Emerging Discipline”, Molecular Systems Biology 2, 2006 0028, 2006.
5 Enriquez, J., “Genomics and the World’s Economy”, Science 281, 925-6, 1998.
6 Aguilar, A., L. Bochereau y L. Matthiessen, “Biotechnology as the Engine for the Knowledge-Based Bio-Economy”, Biotechnology & Genetic Engineering Reviews 26, 371-88, 2010.
7 oecd, The Knowledge-Based Economy, oecd, París, 1996.
8 Fundación Este País, México ante el reto de la economía del conocimiento, Ciudad de México, 2008.
9 Aerni, P., “Agricultural Biotechnology and its Contribution to the Global Knowledge Economy”, Advances in Biochemical Engineering/Biotechnology 107, 69-96, 2007.
10 oecd, “The Bioeconomy to 2030. Designing a Policy Agenda”, oecd, París, 2009.
11 Phillips, K.A., S.Y. Liang y S. Van Bebber, “Challenges to the Translation of Genomic Information into Clinical Practice and Health Policy: Utilization, Preferences and Economic Value”, Current Opinion in Molecular Therapeutics 10, 260-6, 2008.
12 Wetterstrand, K., “dna Sequencing Costs: Data from the nhgri Large-Scale Genome Sequencing Program”, disponible en http://www.genome.gov/sequencingcosts, consultado el 22 de abril de 2011.
13 Lander, E.S., “Initial Impact of the Sequencing of the Human Genome” Nature 470, 187-97, 2011.
14 Wang, L., H.L. McLeod y R.M. Weinshilboum, “Genomics and Drug Response”, The New England Journal of Medicine 364, 1144-53, 2011.
15 Strauss, S., “Biotech Breeding Goes Bovine” Nature Biotechnology 28, 540-3, 2010.
16 Fischhoff, D.A. y M.N. Cline, “Practical Delivery of Genes to the Marketplace”, Methods in Molecular Biology 513, 305-20, 2009.
17 Venter, J.C., “Multiple Personal Genomes Await”, Nature 464, 676-7, 2010.
18 Green, E.D. y M.S. Guyer, “Charting a Course for Genomic Medicine from Base Pairs to Bedside”, Nature 470, 204-13, 2011.
19 who, Genomics and World Health. Report of the Advisory Committee on Health Research, World Health Organization, Geneva, 2002.
20 Nagy, E., E. Urban, J. Soki, G. Terhes y K. Nagy, “The Place of Molecular Genetic Methods in the Diagnostics of Human Pathogenic Anaerobic Bacteria. A Minireview”, Acta Microbiologica et Immunologica Hungarica 53, 183-94, 2006.
21 Patel, S.J. y P.L. Graham, 3rd. “Use of Molecular Typing in Infection Control”, The Pediatric Infectious Disease Journal 26, 527-9, 2007.
22 Joseph, S.J. y T.D. Read, “Bacterial Population Genomics and Infectious Disease Diagnostics”, Trends in Biotechnology 28, 611-8, 2010.
23 Jiménez-Sánchez, G., B. Childs y D. Valle, “The Effect of Mendelian Disease on Human Health” en The Metabolic and Molecular Basis of Inherited Disease., vol. I (eds. C.R. Scriver, A.L. Beaudet, W.S. Sly y D. Valle), McGraw Hill, New York, 2001.
24 Evans, W.E. y M.V. Relling, “Pharmacogenomics: Translating Functional Genomics into Rational Therapeutics”, Science 286, 487-91, 1999.
25 Emilien, G., M. Ponchon, C. Caldas, O. Isacson y J.M. Maloteaux, “Impact of Genomics on Drug Discovery and Clinical Medicine”, Qjm 93, 391-423, 2000.
26 Cochrane, G., I. Karsch-Mizrachi y Y. Nakamura, “The International Nucleotide Sequence Database Collaboration”, Nucleic Acids Research 39, D15-8, 2011.
27 Moser, G., M.S. Khatkar, B.J. Hayes y H.W. Raadsma, “Accuracy of Direct Genomic Values in Holstein Bulls and Cows Using Subsets of snp Markers”, Genetics, Selection, Evolution: GSE 42, 37, 2010.
28 Williamson, J.F. et ál., “Genomic Evolution in Domestic Cattle: Ancestral Haplotypes and Healthy Beef”, Genomics, 19 feb. 2011.
29 Ward, R.D., R. Hanner y P.D. Hebert, “The Campaign to dna Barcode All Fishes, fish-bol”, Journal of Fish Biology 74, 329-56, 2009.
30 Mazur, B., E. Krebbers y S. Tingey, “Gene Discovery and Product Development for Grain Quality Traits”, Science 285, 372-5, 1999.
31 Pieper, D.H., V.A. Martins dos Santos y P.N. Golyshin, “Genomic and Mechanistic Insights into the Biodegradation of Organic Pollutants”, Current opinion in biotechnology 15, 215-24, 2004.
32 Weber, W. y M. Fussenegger, “The Impact of Synthetic Biology on Drug Discovery”, Drug Discovery Today 14, 956-63, 2009.
33 Schirmer, A., M.A. Rude, X. Li, E. Popova y S.B. del Cardayre, “Microbial Biosynthesis of Alkanes”, Science 329, 559-62, 2010.
34 Dellomonaco, C., F. Fava y R. González, “The Path to Next Generation Biofuels: Successes and Challenges in the Era of Synthetic Biology”, Microbial Cell Factories 9, 3, 2010.
35 Kaye, J., N. Hawkins y J. Taylor, “Patents and Translational Research in Genomics”, Nature Biotechnology 25, 739-41, 2007.
36 Kim, W.C. y R. Mauborgne, “Fair Process: Managing in the Knowledge Economy”, Harvard Business Review 75, 65-75, 1997.
37 oecd, oecd Science, Technology and Industry Outlook, oecd Publishing (http://dx.doi.org/10.1787/sti_outlook-2010-en).
38 González, V. et ál., “The Partitioned Rhizobium Etli Genome: Genetic and Metabolic Redundancy in Seven Interacting Replicons”, Proc Natl Acad Sci U S A 103, 3834-9, 2006.
39 Aguilar-Díaz, H. et ál., “The Genome Project of Taenia Solium”, Parasitol Int 55 Suppl, S127-30, 2006.
40 Jiménez-Sánchez, G., I. Silva-Zolezzi, A. Hidalgo y S. March, “Genomic Medicine in Mexico: Initial Steps and the Road Ahead”, Genome Res 18, 1191-8, 2008.
41 Palacios, R. y J. Collado-Vides, “Development of Genomic Sciences in Mexico: A Good Start and a Long Way to Go”, PLoS Comput Biol 3, 1670-3, 2007.
42 Salamanca, F. y S. Armendares, “The Development of Human Genetics in Mexico”, Arch Med Res 26 Spec No, S55-62, 1995.
43 Jiménez-Sánchez, G., “Developing a Platform for Genomic Medicine in Mexico”, Science 300, 295-6, 2003.
44 Jiménez-Sánchez, G., J. Valdés Olmedo y G. Soberón, “Desarrollo de la medicina genómica en México”, Este País 139, 17-23, 2002.
45 Jiménez-Sánchez, G., J. Valdés Olmedo y G. Soberón, “El Instituto Nacional de Medicina Genómica”, Este País 141, 50-56, 2002.
46 Jiménez-Sánchez, G., J. Frenk y G. Soberón, “La primera década de la medicina genómica en México (1999-2009): Hacia un nuevo paradigma en el cuidado de la salud” en El pasado del presente. Miradas y perspectivas (ed. E. Matos Moctezuma), El Colegio Nacional, Ciudad de México, 2010.
47 Silva-Zolezzi, I. et ál., “Analysis of Genomic Diversity in Mexican Mestizo Populations to Develop Genomic Medicine in Mexico”, Proc Natl Acad Sci U S A 106, 8611-6, 2009.
48 OECD, OECD Reviews of Innovation Policy: Mexico 2009, OECD Publishing, 2009.







[…] información, desde secuencias (meta)genómicas hasta modelos ecosistémicos, en el caso del Ecuador, es el resultado de miles, o millones de años […]